|
医疗器械咨询据《国家药品监督管理局2021年度医疗器械注册工作报告》2021年,国家药监局共批准医疗器械首次注册、延续注册和变更注册11314项,与2020年相比注册批准总数量增长14.9%。
其中,首次注册1710项,与2020年相比增加8.8%。延续注册6939项,与2020年相比增加25.6%。变更注册2665项,与2020年相比减少3.1%。
2021年,企业自行撤回注册申请182项,自行注销注册证书49项。
近8年国家药监局批准医疗器械注册情况见图5。
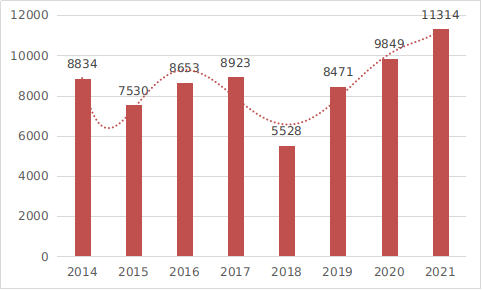
图5 2014至2021年度注册数据图
(一)整体情况
2021年,国家药监局批准境内第三类医疗器械注册4596项,与2020年相比增加27.6%,进口医疗器械6718项,与2020年相比增加7.6%。
按照注册品种区分,医疗器械7844项,占全部医疗器械注册数量的69.3%;体外诊断试剂3470项,占全部医疗器械注册数量的30.7%。
按照注册形式区分,首次注册1710项,占全部医疗器械注册数量的15.1%;延续注册6939项,占全部医疗器械注册数量的61.3%;变更注册2665项,占全部医疗器械注册数量的23.6%。注册形式比例情况见图6。
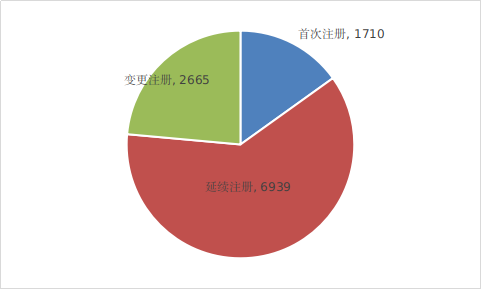
图6 2021年注册形式比例图
(二)分项情况
1.境内第三类医疗器械注册审批情况
境内第三类医疗器械注册4596项。其中,医疗器械3079项,体外诊断试剂1517项。
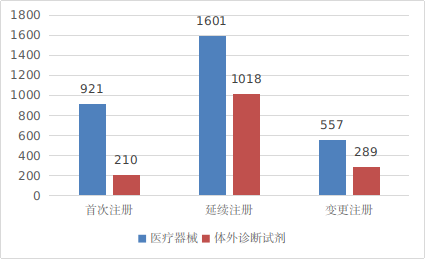
图7 境内第三类医疗器械注册形式分布图
从注册形式看,首次注册1131项,占全部境内第三类医疗器械注册数量的24.6%,延续注册2619项,占全部境内第三类医疗器械注册数量的57%;许可事项变更注册846项,占全部境内第三类医疗器械注册数量的18.4%。注册形式分布情况见图7。
2.进口第二类医疗器械注册审批情况
进口第二类医疗器械注3649项。其中,医疗器械注册2132项,体外诊断试剂注册1517项。
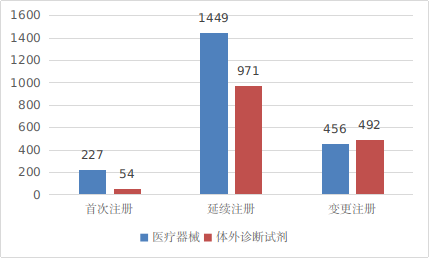
图8 进口第二类医疗器械注册形式分布图
从注册形式看,首次注册281项,占全部进口第二类医疗器械注册数量的7.7%;延续注册2420项,占全部进口第二类医疗器械注册数量的66.3%;许可事项变更注册948项,占全部进口第二类医疗器械注册数量的26%。
|