|
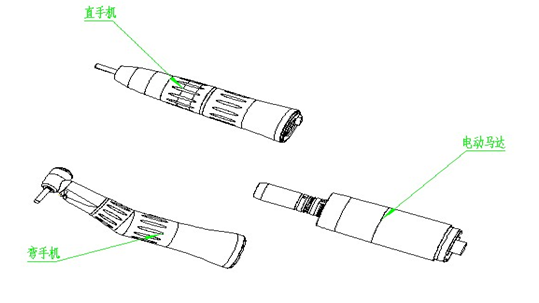
医疗器械注册牙科手机整体结构
医疗器械牙科手机产品注册标准的审查是产品主要技术性能指标审查中最重要的环节之一。
本条款给出需要考虑的产品基本技术性能指标,给出了推荐要求,企业可参考相应的国家标准、行业标准,根据企业自身产品的技术特点制定相应的标准,但不得低于相关强制性国家标准、行业标准的有关要求。
如有不适用条款(包括国家标准、行业标准要求),企业在标准的编制说明中必须说明理由。
1.正常工作条件
企业提交的正常工作条件应包含以下内容,推荐性数据如下,企业可根据自身产品的技术特点规定相应工作条件。
1.1环境温度 5℃~40℃;
1.2相对湿度 ≤80%;
1.3大气压力 86kPa~106kPa;
1.4电源 若适用,按制造商规定;
1.5水压 200kPa~400kPa;
1.6手机接头气源气压范围200 kPa~700 kPa,流量不小于50L/min。
2.性能指标
2.1高速气涡轮手机
应符合YY 1045.1-2009《牙科手机 第1部分:高速气涡轮手机》的规定。
接头(或快速接头)应符合YY/T 0514-2009《牙科手机 软管连接件》,接头输入气压应符合企业的标称值。
2.2低速气动马达手机
2.2.1直手机、弯手机
应符合YY 1045.2-2010《牙科手机 第2部分:直手机和弯手机》的规定。
2.2.2气动马达(如有)
应符合YY 0837-2011 《牙科手机 牙科气动马达》的规定。
2.3电动马达手机
2.3.1直手机、弯手机
应符合YY 1045.2-2010《牙科手机 第2部分:直手机和弯手机》的规定。
2.3.2电动马达(如有)
应符合YY 0836-2011 《牙科手机 牙科低电压电动马达》的规定。
2.4其他配件
如有其他配件(如照明灯),应符合相应的国家标准、行业标准的要求,或制定相应的技术要求。
2.5电气安全性能
以下要求只适用于供电电压不超过安全特低电压的情况。对于非安全特低电压供电的情况,不适用以下要求,应根据产品实际情况满足电气安全要求。
2.5.1申报手机、接头、气动马达如带光照供电,应符合GB 9706.1-2007《医用电气设备 第1部分:安全通用要求》的要求。
2.5.2 电动马达应符合GB 9706.1-2007《医用电气设备第1部分:安全通用要求》 以及YY 0836-2011《牙科手机 牙科低电压电动马达》的要求。
2.5.3其他情况:高速气涡轮手机、低速气动马达手机,若不带光照供电部分,不需引用电气安全标准。
2.6环境试验要求
带光照供电或电动马达驱动的牙科手机的环境试验应符合法规标准GB/T 14710-2009《医用电器设备环境要求及试验方法》中气候环境试验Ⅱ组、机械环境试验Ⅱ组的要求。
2.7电磁兼容
带光照供电或电动马达驱动的牙科手机应符合法规标准YY 0505-2012《医用电气设备 第1-2部分:安全通用要求并列标准:电磁兼容要》的要求。
医疗器械产品注册,医疗器械生产许可证及一类医疗器械备案代理找鸿远医疗器械咨询为您提供一站式服务!
|