|
境内第三类医疗器械注册证书变更审批
一、项目名称:国产医疗器械注册
二、许可内容:境内第三类医疗器械注册证书变更审批:
(一)生产企业实体不变,企业名称改变;
(二)生产企业注册地址改变;
(三)生产地址的文字性改变;
(四)产品名称、商品名称的文字性改变;
(五)型号、规格的文字性改变;
(六)产品标准的名称或者代号的文字性改变
三、实施依据:《医疗器械监督管理条例》、《医疗器械注册管理办法》
四、收费:不收费
五、数量限制:本许可事项无数量限制
六、申请人提交材料目录:
(一) 生产企业实体不变,企业名称改变:
资料编号1、医疗器械注册证变更/补办申请表;
资料编号2、医疗器械注册证书原件;
资料编号3、新的生产企业许可证;
资料编号4、新的营业执照;
资料编号5、新的产品标准(适用于标准主体变更的);
资料编号6、生产企业关于变更的情况说明以及相关证明材料;
资料编号7、所提交材料真实性的自我保证声明;
资料编号8、相应要素未发生改变的声明。
(二)生产企业注册地址改变和生产地址的文字性改变:
资料编号1、医疗器械注册证变更/补办申请表;
资料编号2、医疗器械注册证书原件;
资料编号3、新的生产企业许可证;
资料编号4、新的营业执照;
资料编号5、生产企业关于变更的情况说明以及相关证明材料;
资料编号6、所提交材料真实性的自我保证声明。
(三)产品名称、商品名称文字性改变,产品型号、规格文字性改变以及产品标准的名称或者代号文字性改变:
资料编号1、医疗器械注册证变更/补办申请表;
资料编号2、医疗器械注册证书原件;
资料编号3、新的产品标准;
资料编号4、医疗器械说明书;
资料编号5、生产企业关于变更的情况说明以及相关证明材料;
资料编号6、所提交材料真实性的自我保证声明;
资料编号7、其他。
七、对申报材料的要求:
(一)申报资料的一般要求:
1、申报资料首页为申报资料项目目录,目录中申报资料项目按《医疗器械注册管理办法》附件10的顺序排列。每项资料加封页,封页上注明产品名称、申请人名称,右上角注明该项资料名称。各项资料之间应当使用明显的区分标志,并标明各项资料名称或该项资料所在目录中的序号。整套资料应装订成册。
2、申报资料一式一份,申报资料应使用A4规格纸张打印,内容完整、清楚、不得涂改,政府及其他机构出具的文件按原件尺寸提供。
3、申报资料的复印件应清晰。
4、各项(上市批件、标准、检测报告、说明书)申报资料中的产品名称应与申请表中填写的产品名称实质性内容相对应。若有商品名,应标注商品名。申报资料应当使用中文,根据外文资料翻译的申报资料,应当同时提供原文。
(二)申报资料的具体要求:
1、生产企业实体不变,企业名称改变的申报资料要求:
(1)医疗器械注册证变更/补办申请表
①医疗器械注册申请表可下载“医疗器械(体外诊断试剂)注册电子申报软件2010(含使用手册)”;
②医疗器械注册申请表是注册申请的重要资料之一,表内各项应符合填表说明要求。
(2)医疗器械注册证书原件(申请变更时提交复印件,领取变更后的医疗器械注册证书时交回原件)
(3)新的生产企业许可证
(4)新的营业执照
(5)新的产品标准(适用于标准主体变更的)
①两份;
②两份标准一致的声明。
(6)生产企业关于变更的情况说明以及相关证明材料
(7)所提交材料真实性的自我保证声明
应当包括所提交材料的清单、生产企业承担法律责任的承诺。
(8)相应要素未发生改变的声明
生产企业应提交生产地址、生产条件、产品标准等相应要素未发生改变的声明。
2、生产企业注册地址改变和生产地址文字性改变的申报资料要求:
(1)医疗器械注册证变更/补办申请表
①医疗器械注册申请表可下载“医疗器械(体外诊断试剂)注册电子申报软件2010(含使用手册)”;
②医疗器械注册申请表是注册申请的重要资料之一,表内各项应符合填表说明要求。
(2)医疗器械注册证书原件(申请变更时提交复印件,领取变更后的医疗器械注册证书时交回原件)
(3)新的生产企业许可证
(4)新的营业执照
(5)生产企业关于变更情况的说明以及相关证明文件
(6)所提交材料真实性的自我保证声明
应当包括所提交材料的清单、生产企业对承担法律责任的承诺。
3、产品名称、商品名称文字性改变,产品型号、规格文字性改变以及产品标准的名称或者代号文字性改变的申报资料要求:
(1)医疗器械注册证变更/补办申请表
①医疗器械注册申请表可从下载“医疗器械(体外诊断试剂)注册电子申报软件2010(含使用手册)”;
②医疗器械注册申请表是注册申请的重要资料之一,表内各项应符合填表说明要求。
(2)医疗器械注册证书原件(申请变更时提交复印件,领取变更后的医疗器械注册证书时交回原件)
(3)新的产品标准
①两份;
②两份标准一致的声明。
(4)医疗器械说明书
(5)生产企业关于变更的情况说明以及相关证明材料
(6)所提交材料真实性的自我保证声明
应当包括所提交材料的清单、生产企业承担法律责任的承诺。
(7)其他
对于型号、规格的文字性改变,生产企业应提交文件,声明对变更前后产品的同一性负责。
八、申办流程示意图:
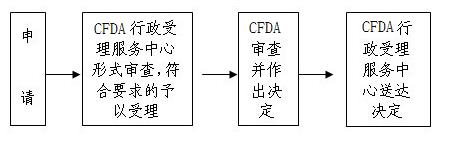
九、许可程序:
(一)受理:
申请人向行政受理服务中心提出申请,按照本《须知》第六条所列目录提交申请材料,受理中心工作人员按照《境内第三类、境外医疗器械产品注册申报资料受理标准》(国药监械[2005]111号)的要求对申请材料进行形式审查。申请事项依法不需要取得行政许可的,应当即时告知申请人不受理;申请事项依法不属于本行政机关职权范围的,应当即时作出不予受理的决定,并告知申请人向有关行政机关申请;申请材料存在可以当场更正的错误的,应当允许申请人当场更正;申请材料不齐全或者不符合法定形式的,应当当场或者在五日内一次告知申请人需要补正的全部内容,逾期不告知的,自收到申请材料之日起即为受理;申请事项属于本行政机关职权范围,申请材料齐全、符合法定形式,或者申请人按照本行政机关的要求提交全部补正申请材料的,应当受理行政许可申请。
(二)许可决定:
行政受理服务中心受理后,即将申请材料送交国家食品药品监督管理总局进行行政审批,国家食品药品监督管理总局在20日内作出予以批准或者不予批准的决定,不予批准的,应当书面说明理由。
(三)送达:
自行政许可决定作出之日起10日内,CFDA行政受理服务中心将行政许可决定送达申请人。
十、承诺时限:
自受理之日起,20日内作出行政许可决定。
十一、实施机关:
实施机关:国家食品药品监督管理总局
受理地点:国家食品药品监督管理总局行政受理服务中心
十二、事项变更:
医疗器械产品注册证书所列内容发生变化的,持证单位应当自发生变化之日起30日内,申请办理变更手续或者重新注册。
十三、许可证件有效期与延续:
变更后的医疗器械注册证书的有效期截止日与原医疗器械注册证书的有效期截止日相同,有效期满应当申请重新注册。
十四、许可年审或年检:无
十五、受理咨询与投诉机构:
咨询:国家食品药品监督管理总局
投诉:国家食品药品监督管理总局驻局监察局、法制司
注:本须知工作期限以工作日计算,不含法定节假日
本文来源于:深圳鸿远医疗器械咨询有限公司 http://www.hongyuanyixiezixun.com
|