|
2023年医疗器械注册申报资料准备要求:
一、注册申报资料依据
《关于公布医疗器械注册申报资料要求和批准证明文件格式的公告》(2021年第121号)
《关于公布体外诊断试剂注册申报资料要求和批准证明文件格式的公告》(2021年第122号)
《关于发布医疗器械注册电子申报目录文件夹结构的通告》(2021年第15号)
《关于实施医疗器械注册电子申报的公告》(2019年第46号)
二、医疗器械注册申报相关要求





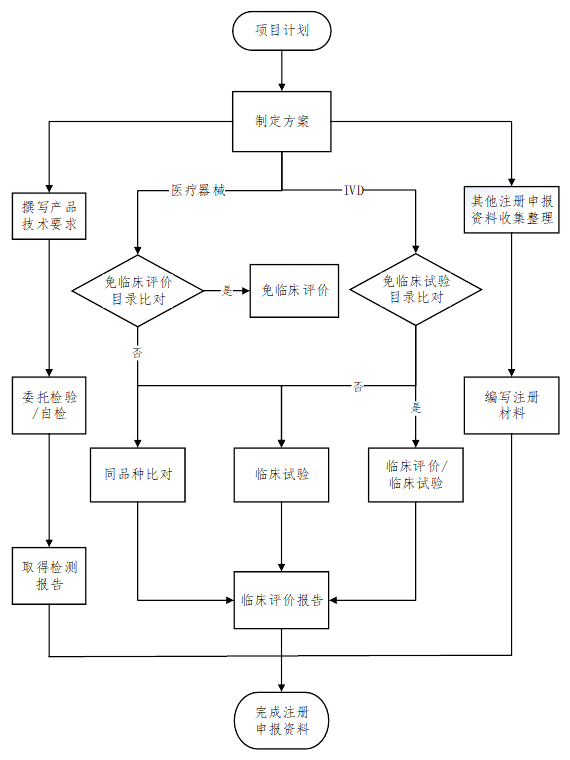
三、医疗器械产品注册申报资料准备流程
深圳鸿远医疗器械咨询有限公司是一家技术专业的医疗器械咨询公司,专注提供全国各地如:深圳、广州、东莞、中山、佛山、潮州、顺德、广西、上海、西安、重庆、成都等知名城市的医疗器械领域技术咨询服务。鸿远医疗器械咨询专业服务于:医疗器械产品注册证、医疗器械生产许可证、进口医疗器械注册、一类医疗器械产品备案及生产备案代办、医疗器械经营许可证代办、二类医疗器械经营备案、医疗器械分类界定、CE认证、ISO13485认证、FDA注册、临床试验、医疗器械质量管理体系认证及体系建立与过程确认文件建立(ISO9001, ISO13485, GMP, CE,QSR820,CMDCAS);产品技术要求制订、技术文件、临床试验及免临床同类产品比对比资料编写、注册资料编写辅导、电磁兼容预测整改、医疗器械广告批文申报、医疗器械出口销售证明办理、洁净室建设指导等提供一站式服务,技术专业,诚信服务,老师手机及微信号:13590396780欢迎您咨询!
|