|
医疗器械咨询据国家药监局关于发布医疗器械动物试验研究注册审查指导原则 第一部分:决策原则(2021年修订版)等2项注册审查指导原则的通告(2021年第75号)
为加强医疗器械产品注册工作的监督和指导,进一步提高注册审查质量,国家药品监督管理局组织制定了《医疗器械动物试验研究注册审查指导原则 第一部分:决策原则(2021年修订版)》《医疗器械动物试验研究注册审查指导原则 第二部分:试验设计、实施质量保证》,现予发布。
《国家药监局关于发布医疗器械动物实验研究和腹腔内置疝修补补片动物实验2项技术审查指导原则的通告》(2019年第18号)发布的《医疗器械动物实验研究技术审查指导原则 第一部分:决策原则》同时废止。
附件1
医疗器械动物试验研究注册审查指导原则第一部分:决策原则(2021年修订版)
医疗器械安全性和有效性评价研究应采用科学、合理的评价方法,其中动物试验是重要手段之一,其属于产品设计开发中的重要研究,可为产品设计定型提供相应的证据支持;若需开展临床试验,可为医疗器械能否用于人体研究提供支持,降低临床试验受试者及使用者的风险以及为临床试验设计提供参考。
但并不是所有医疗器械均需要通过动物试验验证产品安全性和有效性。为了对开展动物试验的必要性判定提供指导,减少动物试验研究数量,避免开展不必要的动物试验,特制订本指导原则。
本指导原则为医疗器械动物试验研究技术审查指导原则系列中的第一部分,为判定是否开展医疗器械动物试验的决策原则,关于动物试验设计等其他方面的内容请参见其他部分指导原则。
本指导原则是供申请人和技术审评人员使用的技术指导性文件,不涉及注册审批等行政事项,亦不作为法规强制执行,如有能够满足法规要求的其他方法,也可以采用,但应提供充分的研究资料和验证资料。应在遵循相关法规的前提下使用本指导原则。
本指导原则是在现行法规和标准体系以及当前认知水平下制订的,随着法规和标准的不断完善,以及科学技术的不断发展,本指导原则相关内容也将进行适时地调整。
一、适用范围
本指导原则适用于决策医疗器械是否需在活体动物上进行在体试验,不包括在非活体动物、离体组织或器官上进行的研究。
以下情况可参考本指导原则:
(一)医疗器械注册申请人在设计开发阶段确定是否需要开展动物试验时;
(二)医疗器械监管机构在技术审评环节评价开展动物试验的必要性时。
本指导原则不替代GB/T 16886系列标准等医疗器械生物学评价相关的技术文件。如通过动物试验方式评价医疗器械的生物相容性,亦应符合GB/T 16886系列标准等生物学评价相关技术文件。
如有针对特定产品的指导原则发布,则遵循相应产品的指导原则。
本指导原则不适用于按照医疗器械管理的体外诊断试剂。
医疗器械临床试验伦理审查时,可参考本指导原则中适用部分以评估临床前动物试验的必要性。
二、基本决策原则
在医疗器械设计开发阶段,决策是否开展动物试验时,建议考虑动物福利伦理原则及风险管理原则。
(一)动物福利伦理原则
申请人需遵循动物试验的“替代(Replacement)、减少(Reduction)和优化(Refinement)”原则,即3R原则。
医疗器械注册办理申请人在决策是否开展动物试验前,需要特别考虑动物福利伦理,充分开展实验室研究,不宜采用动物试验替代实验室研究。
若有经过确认/验证的非活体研究、计算机模拟等方法,则优先采用上述方法以替代动物试验。
申请人宜充分利用已有的信息获取产品安全性、有效性和可行性的相关证据,如可利用已有的同类产品动物试验数据或通过与市售同类产品进行性能比对等方式验证产品的安全性、有效性和可行性。若相关证据充分,可免于动物试验。
(二)风险管理原则
医疗器械产品注册办理申请人在医疗器械设计开发时应进行充分的风险管理活动。风险控制作为风险管理的重要部分,是将风险降低并维持在规定水平的过程。实施每一项风险控制措施后应对其有效性予以验证(其中包括确认活动)。实验室研究或动物试验等均是验证风险控制措施有效性的手段,申请人宜尽可能地通过前期研究(如实验室研究等)对已识别风险的控制措施有效性进行验证,只有在实验室研究不足时,才考虑通过动物试验开展进一步验证。动物试验资料可作为风险/受益分析时的支持性资料。
如需通过动物试验进行风险控制措施有效性的验证,则结合动物试验目的,一般从可行性、有效性、安全性三方面进行考虑:
1.可行性
可行性研究是指产品设计开发阶段进行的,对产品工作原理、作用机理、设计、可操作性、功能性、安全性等方面进行确认/验证,或识别新的非预期风险的研究,如生物可吸收支架平台材料的筛选、经导管瓣膜置换装置的设计可行性、迭代设计更新的验证等。
2.有效性
尽管动物与人体之间,在部分医疗器械的有效性方面可能存在一定差异,但设计合理的动物试验可支持产品的有效性(包括性能和操作),如可吸收防粘连医疗器械的防粘连性能评价,组织修复材料引导组织重建的有效性评价,多孔涂层关节类产品或3D打印多孔结构产品的骨结合效果评价等。
3.安全性
医疗器械注册证申请人采取风险控制措施后,部分产品安全性可适当采用动物试验研究进行评价,如含药医疗器械中药物安全性范围研究,通过组织病理学等方式的毒理学评价、产品对生物体的损伤评价,动物源性材料的抗钙化性能,外科血管闭合设备的血管热损伤研究,防粘连器械与组织粘连相关并发症的评价等。
试验目的有时是不能严格划分界限的,因此一项动物试验可能同时对产品的可行性、有效性、安全性进行评价。
若产品采用新的作用机理、工作原理、设计、主要材料/配方、应用方法(如手术操作)、预期用途、增加新的适用范围、改进某方面性能等,申请人应针对产品创新点相关风险进行评估,并考虑通过动物试验对风险控制措施的有效性进行验证。
医疗器械产品注册证申请人可参考以下决策流程图进行是否开展动物试验的决策。
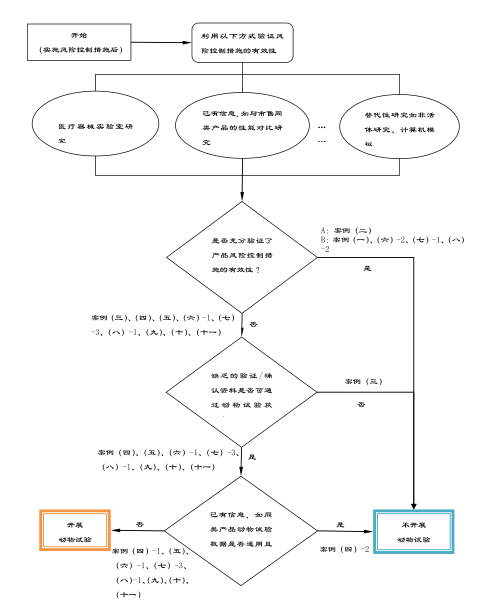
图1 决策开展动物试验的流程图
三、是否开展动物试验的决策案例
附页列出了部分可能需要开展动物试验的产品示例,需要注意的是,在不同的具体情形下,根据决策原则对于同样的产品可能将得出不同的判定结果;另外,对于表中未列的医疗器械产品,在某些具体情形下也可能需要开展动物试验。建议申请人根据产品实际情况参照决策流程图予以判定。
为便于理解决策原则,本章节列举了以下实际案例。相关案例仅针对特定产品在具体情形下的决策判定,例如同一申请人在前代植入式心脏起搏器基础上对产品功能的改进或更新,再例如采用新材料制造的肠道吻合器等。
(一)多孔涂层生物型髋关节假体
多孔涂层生物型髋关节假体的主要风险包括产品骨结合效果欠佳或涂层剥落造成的假体固定失败等,通过动物试验可评价涂层的骨结合效果。如果通过涂层的成分表征、形貌及体视学数据(厚度、孔隙率、孔隙尺度等)、涂层机械性能评价(涂层与基体结合强度等)、涂层稳定性及耐腐蚀性能评价、生物相容性评价等研究证明其与已上市同类产品的涂层具有等同性,则无需通过动物试验来评估多孔涂层的骨结合效果和涂层的稳定性。
(二)心电图机
心电图机的主要风险之一是工作数据的不准确性,包括心电图自动测量的不准确性和心电图自动诊断的不准确性。可进行实验室研究,通过心电图标准数据库来验证心电图自动测量的准确性,可通过形态诊断用心电图数据库和节律诊断用心电图数据库来确认公开形态解释的准确性和公开节律诊断的准确性,无需开展动物试验。
(三)注射用交联透明质酸钠凝胶
交联透明质酸钠凝胶可用于面部注射以纠正鼻唇沟皱纹,纠正效果一般可达到6个月。鉴于通过动物试验无法考察人体面部皱纹的改善程度,故一般不采用动物试验数据支持该类产品的有效性,建议在人体临床评价资料中关注产品注射6个月时的鼻唇沟皱纹严重程度分级(如WSRS)较术前的改善程度等疗效评价指标。
(四)可吸收生物疝修补补片
本案例提及的可吸收生物疝修补补片用于修复腹壁疝及腹壁缺损,一般具有类似细胞外基质的微观结构。产品植入人体后,宿主细胞在材料中生长,最终重塑出的腹壁组织对缺损进行修补。
1.该类产品最主要的风险之一在于疝或腹壁缺损的复发,宜采取一系列风险控制措施确保产品组织重建的有效性,以降低疝复发的风险。对于该类产品,仅仅依靠常规的实验室研究并不能验证疝复发风险相关控制措施的有效性,宜考虑使用组织病理学等动物试验数据验证组织重建效果。
2.医疗器械注册证办理申请人在开展动物试验前可收集已有同类产品的动物试验资料或文献数据,并分析这些数据能否用于支持申报产品组织重建效果的评价,如现有资料充分则无需开展动物试验。
(五)体外除颤产品
体外除颤产品供不同的使用者和操作者在不同的预期使用环境下进行体外电复律治疗。
对于该类产品,常规的实验室研究并不能验证体外电复律技术风险相关控制措施的有效性,因此宜使用活体动物开展试验获得除颤研究数据进行验证。
(六)超声软组织切割止血系统
超声软组织切割止血系统用于软组织切割和血管闭合产品通过摩擦产生的热量导致组织凝固后被切开、封闭血管(本例子不包含3mm以上血管的切割和闭合功能的特殊要求)。
1.该产品主要风险包括产品设计不合理等原因可能造成的血管切割闭合不充分和组织热损伤等。仅依靠实验室研究无法充分验证这些风险的控制措施是否有效,需要通过急性动物试验观察产品的即刻的血管切割闭合情况和组织热损伤情况,需要通过慢性动物试验观察热损伤愈合情况和继发出血情况,进而验证风险控制措施的有效性。
2.若申请的产品包含多个类似设计的刀头,可在开展动物试验前通过体外爆破压力实验筛选出性能最差的刀头开展动物试验,以起到减免部分动物试验的目的。对于新增与已有刀头相似(设计类似、性能相近)的刀头,可使用体外爆破压力实验结果证明其与相似刀头的等同性,不再开展动物试验。
(七)植入式心脏起搏器
1.植入式心脏起搏器属于高风险植入器械,开展动物试验可以为产品设计定型提供相应的证据支持。若同一申请人在前代产品基础上进行植入式心脏起搏器的改进或更新,对于前代产品已验证的内容无需开展动物试验,必要时申请人仅针对改进或更新部分开展相应的动物试验。
2.患者在植入心脏起搏器后一般不能进行核磁共振检查(MRI),如果申请人设计开发了MRI兼容的植入式心脏起搏器,需要评估MRI环境对产品安全性及有效性带来的影响,进行MRI兼容性相关研究。MRI兼容性研究通常需要应用动物进行计算机建模验证MRI兼容的安全性与有效性,当验证过计算机建模的准确性后,对于同一申请人其他植入式心脏起搏器产品的MRI兼容性研究,可以不再重复进行动物试验。
3.无导线起搏器与传统的植入式心脏起搏器相比,采用了新的结构设计、手术操作方法,不需要植入传统的植入式心脏电极导线,申请人宜针对创新点相关风险进行评估,并对风险控制措施有效性进行验证或确认,申请人宜对无导线起搏器开展动物试验,验证产品安全性、有效性及可行性。
(八)药物洗脱支架
1.尽管药物洗脱支架产品所含药物如紫杉醇、雷帕霉素已作为药品具有较长的临床应用历史,但在器械中应用与其单独作为药品应用时具有较大差异,例如药物洗脱支架植入后,靶血管壁中的局部组织药物浓度会远远高于药品系统使用后的血药浓度,单纯作为药品使用的药代及毒理学研究资料并不足以支持其安全性,宜进一步通过动物试验开展靶血管、远端心肌等局部组织的毒理学安全性研究,获取必要的组织病理学数据等。对于两个含有相同药物的药物洗脱支架,若支架药物载体材料不同,临床应用时同样存在较大差异,例如药物成分从不同载体材料中释放、吸收的速率不同,宜通过动物试验研究结合已有的文献数据资料来确认药物剂量密度及安全范围。
2.对于涂有可降解涂层的药物洗脱支架产品,其降解性能是载体聚合物材料筛选中一项重要因素。通过动物试验在体研究药物洗脱支架涂层的降解性能十分必要,但如果载体聚合物(例如聚乳酸-羟基乙酸共聚物,PLGA)的降解性能,可通过同类产品信息、文献数据信息、材料数据库信息、监管机构备案信息等获得支持,申请人无需对申报产品重新开展降解性能的动物试验。
(九)骨内固定用可降解金属螺钉
骨内固定用可降解金属螺钉,该类产品在骨愈合初期提供初始的稳定固定,待骨愈合后逐渐降解,避免二次手术取出。
该类产品主要风险包括降解周期与骨愈合周期不匹配造成内固定过早失效,以及降解产物对机体组织和器官带来的安全性问题等。对于该类产品,仅仅依靠常规的实验室研究并不能验证失效风险相关控制措施的有效性,需要通过适宜的动物模型的相应部位制备骨折或骨缺损模型,评价可降解金属产品在适宜的动物体内的降解性能和产品的安全性及有效性。具体试验项目可包含X光评价、血液中元素分析、组织病理分析、micro-CT分析、植入生物力学评价、周围骨组织分析等。
(十)吻合器
吻合器主要用于组织/脏器的切除、闭合。
1.用于实质脏器或血管切割/吻合的吻合器类产品,因常规的实验室研究并不能充分验证吻合器用于人体的操作性能和吻合性能,宜开展动物试验。
2.对于采用了新材料的肠道或皮肤吻合器类产品,若产品性能、吻合钉材质等与已上市产品存在差异性,仅依靠常规的实验室研究和现有数据不足以评价产品安全性和有效性,宜开展动物试验。另外,通过动物试验可确定产品临床相关参数(如组织厚度等),预测产品在人体中使用时可能出现的安全性问题。
(十一)可吸收外科防粘连产品
对于可吸收外科防粘连产品,应实现产品预期的防粘连功能。该功能宜在适当的活体动物模型上进行研究。动物试验中宜尽可能地体现手术方法、特定手术部位、粘连的类型、粘连的评价方式,以及拟在临床应用时的产品使用方法,并观察产品是否能有效降低粘连的发生率、广泛程度及严重程度等。另外,通过动物试验也可以更好地为临床研究方案设计提供参考。
四、参考资料
[1] General Considerations for Animal Studies for Medical Devices [EB].(Draft Guidance)
[2] EFS Guidance: Investigational Device Exemptions (IDEs) for Early Feasibility Medical Device Clinical studies, Including Certain First in Human (FIH) Studies[EB].
[3] Recommended Content and Format of Test Reports for Complete Non-Clinical Bench Performance Testing in Premarket Submissions [EB].(Draft Guidance)
[4] 《超声软组织切割止血系统技术审查指导原则》(2018年第37号通告)
[5] 《腔镜用吻合器产品注册技术审查指导原则》(2017年第44号通告)
[6] 《腹腔、盆腔外科手术用可吸收防粘连产品注册技术审查指导原则》(2016年第7号通告)
[7] 《冠状动脉药物洗脱支架临床前研究指导原则》(2018年第21号通告)
[8] 《体外除颤产品注册技术指导原则》(2017年第6号通告)
[9] 《腹腔内置疝修补补片动物实验技术审查指导原则》(2019年第18号通告)
[10] 《钙磷/硅类骨填充材料注册技术审查指导原则》(2017年第14号通告)
[11] 《无源植入性医疗器械临床试验审批技术审查指导原则》(2018年第40号通告)
[12] YY/T 0316-2016《医疗器械 风险管理对医疗器械的应用》
[13]ISO 14971:2007 Medical devices—Application of risk management to medical devices[S].
[14] “Non-Animal Approaches - The Way Forward”, European Commission Scientific Conference summary report, Mark Cronin, March 2017
[15] Directive 2010/63/EU of The European Parliament And of The Council on the protection of animals used for scientific
医疗器械动物试验研究注册审查指导原则第二部分:试验设计、实施质量保证
医疗器械安全性和有效性评价研究应采用科学、合理的评价方法,其中动物试验是重要手段之一,其属于产品设计开发中的重要研究,可为产品设计定型提供相应的证据支持;若需开展临床试验,可为医疗器械能否用于人体研究提供支持信息,降低临床试验受试者及使用者的风险以及为临床试验设计提供参考。
本指导原则为医疗器械动物试验研究技术审查指导原则系列中的第二部分,旨在进一步指导申请人在最小负担下更高质量地开展医疗器械动物试验研究。申请人宜参照《医疗器械动物试验研究技术审查指导原则第一部分:决策原则》以避免开展不必要的动物试验;当申请人决定开展动物试验时,可参考本指导原则开展研究方案设计、实施质量保证相关工作。
本指导原则是供申请人和技术审评人员使用的技术指导性文件,不涉及医疗器械注册审批等行政事项,亦不作为法规强制执行,如有能够满足法规要求的其他方法,也可以采用,但应提供充分的研究资料和验证资料。应在遵循相关法规的前提下使用本指导原则。
本指导原则系在现行法规和标准体系以及当前认知水平下制订,随着法规和标准的不断完善,以及科学技术的不断发展,本指导原则的相关内容也将适时地进行调整。
一、适用范围
本指导原则适用于医疗器械产品相关的动物试验设计与实施,不适用于在非活体动物、离体组织或器官上进行的研究。
本指导原则不替代GB/T 16886系列标准等医疗器械生物学评价相关的技术文件。如通过动物试验方式评价医疗器械的生物相容性,亦应符合GB/T 16886系列标准等生物学评价相关技术文件。
如有针对特定产品的指导原则发布,则遵循相应产品的指导原则。
本指导原则不适用于按照医疗器械管理的体外诊断试剂。
二、研究方案设计
医疗器械动物试验是根据试验目的,选用符合试验要求的动物,在预先设计研究方案规定下,进行产品可行性和/或安全性和/或有效性研究,观察、记录动物的反应过程及结果,以确认医疗器械对生命活动的作用与影响。动物试验获得的可行性、安全性和有效性数据宜考虑重复性(Repeatability)及再现性(Reproducibility)。
研究方案设计时,宜遵循“替代、减少、优化(3R,Replacement, Reduction and Refinement)”原则,并综合科学、伦理、经济等方面因素进行考虑。在研究方案设计之前宜结合医疗器械预期受益及风险,汇总并分析已有的动物试验资料,包括文献资料、同类产品的动物试验证据等信息。
良好的动物试验设计既能够保证采用尽可能少的动物进行科学的数据分析,又能够科学、合理地评价医疗器械产品可行性、安全性和有效性。申请人宜结合产品的作用机理、工作原理、设计特征等方面进行研究方案设计。
适宜的预试验有助于优化试验设计。已有证据表明试验方法或操作等对研究结果有显著影响如学习曲线效应,在安全性和有效性研究前宜进行预试验。
申请人应提出明确的试验目的(即拟解决的问题),并根据试验目的由具有相应专业知识和实践经验的人员制定科学、合理的研究方案。
研究方案中所有试验方法或操作步骤均宜通过相关操作规范等文件进行详细规定,如出现与研究方案和/或试验方法或操作步骤的偏离,应对偏离内容进行详细说明并分析该偏离对研究结果的影响。
若产品采用新的作用机理、工作原理、设计、主要材料/配方、应用方法(如手术操作),增加新的适用范围、改进某方面性能等,宜针对产品创新点/变化引入的相关新增风险,结合预期用途进行研究方案设计。
(一)试验目的
动物试验研究根据目的一般分为可行性研究、安全性研究和有效性研究,但有时不能严格划分界限,在一项动物试验中可同时对产品的可行性、有效性、安全性进行评价。
1.可行性研究
可行性研究是指在产品设计开发阶段进行的,对产品作用机理、工作原理、设计、可操作性、功能性、初步安全性等方面进行确认,或识别新的非预期风险的研究。
可行性研究可用于评估动物试验中不同研究指标的结果变异性,为安全性和有效性研究的试验设计要素如动物数量等提供设计依据。
对于部分产品如创新性医疗器械,申请人可通过可行性研究识别产品设计方面引入的新增风险,开展相应的风险管理活动,对产品进行完善和改进。
申请人可提供可行性动物试验研究证据,作为产品设计依据的支持性资料。可行性研究并不是必须开展的,对于某些具有较多研究背景信息支持的医疗器械,可直接开展安全性和有效性研究。
2.安全性研究
医疗器械安全性研究一般是动物试验的主要研究目的,评价设计定型产品在实现功能时对机体安全性的影响,可包括短期(如评估操作安全性的即刻研究)、中/长期(如根据植入物降解周期)的安全性试验。
适用时,申请人宜提供安全性动物试验研究资料,作为评价产品安全性的支持性资料。
3.有效性研究
尽管动物与人体之间在有效性评价方面可能存在一定差异,但有些情况下,设计合理的动物试验可支持产品的有效性。如可吸收防粘连医疗器械的防粘连性能评价,组织修复材料引导组织再生和重塑的有效性评价,多孔涂层关节类产品或3D打印多孔结构产品的骨结合效果评价等。
采用动物试验评估产品的有效性,必要时预先对动物和评价指标等与人体的相关性进行分析,如利用已有文献信息、数据库信息、前代产品的动物试验研究资料等。
适用时,申请人宜提供有效性动物试验研究资料,作为评价产品有效性的支持性资料。
(二)受试器械和对照
1.受试器械
申请人应在研究方案中对使用的受试器械进行详细描述,包括名称、结构及组成(含配合使用的附件、产品图示)、型号规格、批号、保存期限、保存条件、单个动物使用数量、使用频次(如适用)、是否重复使用等信息。
动物试验研究过程中,如发生产品设计更改,申请人应详细地描述变化内容,同时分析变化情况对于动物试验过程、试验结果及结论的影响。必要时重新设计、实施动物试验。
在可行性研究中,可采用设计未定型产品作为受试器械,但最终评价产品安全性、有效性动物试验研究中,受试器械一般应为设计定型的终产品。
动物试验中受试器械应当能够代表注册单元内其他产品的安全性和有效性。
如由于动物解剖结构等因素影响,未使用终产品时,需提供合理性分析,确认未对试验结果及结论产生影响。
动物试验中受试器械的操作方法,宜同预期的临床操作方法一致。如采用不同的操作方法,应确认未对试验结果及结论产生影响。
2.对照
申请人宜对是否设立对照组进行分析论证。
若需设立对照组,可根据评价指标特点等选择对照器械和/或对照材料等。宜优先选择已上市的同类器械作为对照,若选择非境内已上市产品,需提供其可作为对照器械的合理理由和证据。
适当时,动物试验中可设立其他适宜对照组,如其他干预手段。
(三)实验用动物
实验用动物的选择对于医疗器械可行性、安全性和有效性评价至关重要。建议优先选择实验动物。
在实验用动物选择时,建议综合考虑以下方面(包括但不限于):
1.动物试验目的
实验动物通常包括常规实验动物、自发突变实验动物和基因工程实验动物等;实验动物种类可包括啮齿类动物如大鼠和小鼠、非人类灵长类动物如猕猴,其他哺乳动物如兔、犬、猪等,申请人宜根据不同的试验目的选择适宜的实验动物。
如钙磷硅类骨填充材料,在研究其在缺损处的成骨效果时,需考虑动物骨骼自身修复能力对试验结果的影响,为了更好地完成该动物试验的研究目的,应选择骨骼发育成熟的动物。
如对于生物可吸收冠状动脉药物洗脱支架产品,在研发早期的产品降解周期、机械性能、降解产物同组织的相容性及组织反应研究中,可选择小型动物(如兔)来开展研究。产品设计定型后的动物试验研究可采用猪作为实验用动物。
2.宜选用标准化的实验动物
标准化的实验动物主要是指对其携带的微生物实行控制,遗传背景明确或者来源清楚且符合相关标准的动物。在医疗器械动物试验研究中,宜尽量选用该类实验动物,如使用尚无标准的实验用动物,应说明选择理由,并分析对试验结果的影响。
3.与人体的相似性、
宜优先考虑结构(如解剖结构、尺寸)、功能、代谢及疾病特点、生物应答等方面与人体的相似性以及对试验结果的影响,动物与人体相似性越高,则动物试验可行性、安全性和有效性分析结果外推至人体水平时,支持的证据水平越高。
不同的动物种属及品种/品系可能具有不同的解剖结构和生理特点,导致生物应答等方面各不相同,因此申请人宜根据试验目的选择适宜种属和品种/品系的动物进行动物试验。
如对于腹腔内置疝修补补片,考虑动物与人体在腹壁解剖结构、新生腹膜化程度等方面的可比性因素,宜选择小型猪、比格犬进行动物试验研究。
如对于体外除颤动物试验,因考虑到猪的心脏在解剖学、组织病理学、血流动力学和心肌侧枝循环分布等方面与人类最为相似,宜选择健康的猪进行体外除颤动物试验研究。
4.评价指标敏感性
选择实验用动物时,宜充分考虑动物与评价指标之间的敏感性关系。如生物型人工心脏瓣膜产品,在钙化水平研究的动物试验中,宜选择低龄动物作为钙化水平研究的实验用动物。
5.动物基本要素
动物性别、规格(年龄、体重)、健康和疾病状态、病原体感染情况等均可能会对动物试验结果和结论造成影响,因此实验用动物选择时宜充分考虑上述因素。
如对于体外除颤设备的动物试验,成人用医疗器械动物试验研究中猪的体重需在30kg~80kg之间,小儿用医疗器械动物试验研究中猪的体重需在4kg~25kg之间。
6.疾病模型的建立
动物试验中宜建立合适的动物疾病模型用于研究,如未建立疾病模型需提供合理的论证。
如通过动物试验评价硬脑膜修补材料的修补效果时,需根据预期用途建立硬脑膜缺损模型。
如对于体外除颤动物试验,宜建立实验用猪的诱发心室颤模型。
7.其他
实验用动物选择时还需考虑环境、营养、动物作息、麻醉方法、手术技巧方法、疾病模型制备方法等因素对试验结论造成的影响。
(四)动物数量
在产品设计研发早期的可行性研究中,由于缺乏较成熟的经验,动物数量可能是预估的,但获得的数据可以为安全性和有效性研究的动物数量提供设计依据。
产品设计定型后开展的安全性和有效性研究,一般可结合明确的研究目的、相应的研究假设(如适用)、文献信息、同类产品经验、可行性研究或预试验结果等方面预估动物数量。虽然可直接采用统计学原则估算样本量,但也可能使动物试验所需的动物数量较多。建议动物数量宜充分保证试验结果具有可靠性,且符合3R原则,可不采用统计学方法来估算数量。若在相同试验条件下,动物个体之间呈现出的评价结果具有较大的变异性,需分析变异性原因,如操作方法、产品质量等,适当时宜增加动物数量来获得更加科学和客观的结论。
动物试验如有多个观察时间点,每一观察点的动物数量均应保证试验结果具有可靠性。建议预估动物数量时,考虑因各种原因导致动物过早死亡的情况。
适当时,可在同一只动物多个组织部位使用器械。
(五)观察时间
动物试验的观察时间宜根据试验目的、产品特点、评价指标来进行设定,同时宜参考同类产品的研究情况。动物试验按照观察时间长短可划分为急性研究和慢性研究,急性研究一般是术后即刻/短期观察的研究;慢性研究一般是术后中/长期观察的研究。申请人宜根据医疗器械产品的作用机理、已有的背景信息等资料确定开展哪种类型的动物试验研究。
在动物试验中宜设置足够的、不同的观察时间点,观察特定时间点的评价指标,评估产品对动物的影响。在研究方案中宜充分说明不同观察时间点设置的合理性,一般可包括术前、术中、术后即刻、术后短期、术后中/长期等。
观察时间点的设置宜考虑医疗器械产品工作原理、预期与人体接触方式和时间、达到生物应答稳态所需时间等方面因素影响。如对于产品腹腔一侧为不可吸收材料的腹腔内置疝修补补片产品,观察时间点宜选择至少28天;对于产品腹腔侧为可吸收材料的产品,宜根据产品预期完全降解或生物应答稳态的时间确定观察时间点。不同评价指标的观察频次可能不同。
当动物试验持续时间较长如生物可吸收冠状动脉药物洗脱支架,申请人结合已有动物试验结果能够充分说明产品的初步安全性和可行性时,可考虑开展人体临床试验,在开展临床试验的同时需继续完成动物试验。
(六)评价指标
研究方案中需预设评价指标,并在预设的观察时间点对评价指标进行观察。
研究方案中需明确评价指标的具体评价方法如影像学、大体解剖、组织病理学、性能测试等;需明确具体评价指标的观察时间点和频次。评价指标宜有科学、客观的评价标准。
动物试验研究中,宜对任何安全性事件/异常进行记录和分析。
如果发生动物死亡,应详细分析死亡的原因,分析同器械相关性。
三、实施与质量保证
医疗器械注册申请人负责发起、申请、组织、监查动物试验,并对动物试验的动物福利伦理、真实性和科学性负责,申请人应保证试验数据完整、真实、可靠、可追溯,结果可信。
应建立相应的动物试验研究质量管理体系,并维护体系保持有效运行,必要时接受监管部门检查。
动物试验通用要求可参考相关国家标准(如GB/T 35823)。
本指导原则仅对动物试验实施与质量保证基本要素进行了建议。
(一)动物试验的实施
医疗器械动物试验应制定试验题目或代号,并在相关的质量管理体系文件及试验记录中统一使用该试验题目或代号。试验中所采集的各种样本均应标注题目或代号、样本编号和采集日期。
应确保动物试验实施全过程中的动物福利保护,动物在试验期间出现健康、疾病等问题时,应及时处理并评估对试验结果的影响。研究方案实施前需经动物伦理委员会批准。
研究方案的主要内容宜包括但不限于:
1.动物试验题目或代号;
2.所有参与研究的研究机构/单位和申请人的名称、地址及联系方式;动物生产和/或使用许可证号(如适用);
3.动物试验项目负责人和参加试验的主要人员姓名和职责;如存在多场所研究的情况下,应当明确负责各部分试验工作的研究场所、主要研究者姓名及其所承担的工作内容;
4.动物试验研究依据的试验标准、指导原则或者文献等;
5.动物试验目的和背景信息(包括产品更改信息);
6.受试器械和对照描述,如名称、缩写名、代号、型号规格、批号、保存期限、保存条件。提供受试器械、对照、型号规格选择的合理性说明等。未设立对照的合理性说明(如适用);
7.实验用药物和配用器械的相关信息,如药物名称和剂量、配用器械名称和型号规格等;
8.实验用动物的种属和品种/品系、性别、规格、来源、动物等级(如适用)、分组方法和识别方法、健康状况等信息;
9.受试器械和对照的使用方法、剂量(如适用)和频次;
10.动物试验评价指标以及检测方法、频次及持续时间;
11.数据统计处理方法;
12.方案偏离处理方法;
13.档案的保存时间和地点。
应严格按照研究方案和相应的操作规范文件,记录试验产生的所有数据,并保证数据记录及时、直接、准确、清晰和不易消除。试验记录需注明记录日期并由记录者签名。记录的数据需要修改时,应当保持原记录清晰可辨,并注明修改的理由及修改日期,并由修改者签名。电子数据的生成、修改也应当符合以上要求,同时保证电子数据具有完整的稽查轨迹和电子签名。
宜建立受试器械和对照接收、保管、使用记录、处理文件,保证样品使用具有可追溯性。
动物试验实施过程中发生的任何偏离试验研究方案和操作规程的情况,都应当及时记录并报告项目负责人,在多场所研究的情况下还应报告给负责相关试验的主要研究者。项目负责人或者主要研究者应评估对研究数据的可靠性造成的影响,必要时采取纠正措施。
医疗器械动物试验总结报告应有质量保证审查,由项目负责人签字批准。总结报告需签章。
动物试验研究总结报告主要内容宜包括但不限于:
1.动物试验题目和代号;
2.所有参与研究的研究机构/单位和申请人的名称、地址和联系方式;动物生产和/或使用许可证号(如适用);
3.动物试验项目负责人和参加试验的主要人员姓名和职责;如存在多场所研究的情况下,应当明确负责各部分试验工作的研究场所、主要研究者姓名及其所承担的工作内容;
4.动物试验研究依据的试验标准、指导原则或者文献;
5.动物试验目的和背景信息(包括产品更改信息);
6.受试器械和对照(如适用)描述,如名称、缩写名、代号、型号规格、批号等;
7.实验用药物和配用器械的相关信息,如药物名称和剂量、配用器械名称和型号规格等;
8.实验用动物的种属和品种/品系、性别、规格、来源、动物合格证或检疫合格证明等同类文件(如适用)、动物等级(如适用)、分组方法和识别方法、健康状况等信息;
9.受试器械和对照的使用方法、剂量(如适用)和频次;
10.动物试验评价指标以及检测方法、频次及持续时间;
11.动物试验测量/观察获得的个体数据及统计数据;分析数据所采用的统计方法;组织病理观察需同时提供彩色病理照片;
12.结果和结论;
13.方案偏离及所有影响研究数据可靠性的情况分析如剔除数据;对异常/非预期安全性事件进行分析如死亡;
14.质量保证声明;
15.项目负责人签署的、陈述研究符合性声明;
16.档案的保存地点。
(二)动物试验的质量保证
应按照已建立的质量管理体系要求,配备足够的质量保证人员负责质量保证工作,并确保质量保证工作的独立性。质量保证人员不能参与具体试验项目的实施,或者承担可能影响其质量保证工作独立性的其他工作。应当制定书面的质量保证计划,并指定执行人员,以确保研究机构/单位的研究工作符合性。
宜对质量保证活动制定相应的操作规程,包括运行、质量保证计划及检查计划的制定、实施、记录和报告,以及相关资料的归档保存等。
动物试验项目实施过程中,质量保证人员应对试验过程的关键阶段进行检查和记录。对于检查中所发现的问题,应及时向项目负责人和机构负责人报告,并对纠正措施进行审核。质量保证检查应当有过程记录和报告,必要时应当提交监管部门检查。
质量保证人员需对动物试验项目进行审核并出具质量保证声明,确认是否准确完整地描述了研究的方法、程序、结果,真实全面地反映研究的原始数据。质量保证声明需包含完整的研究识别信息、相关质量保证检查活动以及报告的日期和阶段。任何对已完成总结报告的修改或者补充应当重新进行审核并签署质量保证声明。质量保证人员在签署质量保证声明前,应当确认试验符合本指导原则的要求,遵照研究方案和操作规程执行,确认总结报告准确、可靠地反映原始数据。
四、术语
1.机构负责人:全面负责某一研究机构的组织和运行管理的人员。
2.项目负责人:全面负责组织实施动物试验研究中某项试验的人员。
3.主要研究者:在多场所研究中,代表项目负责人在分研究场所实施试验的人员。
4.多场所研究:在不同研究机构或者同一研究机构中不同场所内共同实施完成的研究项目。该类研究项目只有一个研究方案、项目负责人,形成一个总结报告,项目负责人和动物所处的研究机构或者场所为“主研究场所”,其他负责实施研究工作的研究机构或者场所为“分研究场所”。
5.偏离:非故意的或者由不可预见的因素导致的不符合研究方案或者操作规程要求的情况。
6.电子数据:任何以电子形式表现的文本、图表、数据、声音、图像等信息,由计算机化系统来完成其建立、修改、备份、维护、归档、检索或者分发的数据。
7.稽查轨迹:按照时间顺序对系统活动进行连续记录,该记录足以重建、回顾、检查系统活动的过程,以便于掌握可能影响最终结果的活动及操作环境的改变。
五、参考文献
[1]秦川,魏泓.实验动物学第二版[M].北京:人民卫生出版社,2015.
[2]《体外除颤产品注册技术指导原则》(2017年第6号通告)
[3]《钙磷/硅类骨填充材料注册技术审查指导原则》(2017年第14号通告)
[4]《冠状动脉药物洗脱支架临床前研究指导原则》(2018年第21号通告)
[5]《超声软组织切割止血系统技术审查指导原则》(2018年第37号通告)
[6]《医疗器械动物试验研究技术审查指导原则第一部分:决策原则》(2019年第18号通告)
[7]《腹腔内置疝修补补片动物实验技术审查指导原则》(2019年第18号通告)
[8]《药物非临床研究质量管理规范》(国家食品药品监督管理总局令第34号)
[9]GB 12279-2008《心血管植入物人工心脏瓣膜》
[10]U.S. Food and Drug Administration. General Considerations for Animal Studies for Cardiovascular Devices[EB],2010.
[11]U.S. Food and Drug Administration. General Considerations for Animal Studies forCardiovascular Devices(Draft)[EB],2015.
[12]Munnelly A.et al.Biomaterial Calcification: Mechanisms and Prevention [M]. In: Eliaz N. (eds) Degradation of Implant Materials.Springer,2012.
[13]Office of Animal Care and Use. Guidelines for Endpoints in Animal Study Proposals[EB],2019.
[14] B Voelkl et al.Reproducibility of preclinical animal researchimproves with heterogeneity of study samples[J]. PLoS Biol,2018.
[15]Kilkenny C et al.Improving Bioscience Research Reporting: The ARRIVE Guidelines for Reporting Animal Research[J].PLoS Biol,2010.
[16] CR Hooijmans et al.A Gold Standard Publication Checklist to Improve the Quality of Animal Studies, to Fully Integrate the Three Rs, and to Make Systematic Reviews More Feasible[J].Altern Lab Anim,2010.
深圳鸿远医疗器械咨询有限公司是一家技术专业的医疗器械咨询公司,专注提供全国各地如:深圳、广州、东莞、中山、佛山、潮州、顺德、广西、上海、西安、重庆、成都等知名城市的医疗器械领域技术咨询服务。鸿远医疗器械咨询专业服务于:医疗器械产品注册证、医疗器械生产许可证、进口医疗器械注册、一类医疗器械产品备案及生产备案代办、医疗器械经营许可证代办、二类医疗器械经营备案、医疗器械分类界定、CE认证、ISO13485认证、FDA注册、临床试验、医疗器械质量管理体系认证及体系建立与过程确认文件建立(ISO9001, ISO13485, GMP, CE,QSR820,CMDCAS);产品技术要求制订、技术文件、临床试验及免临床同类产品比对比资料编写、注册资料编写辅导、电磁兼容预测整改、医疗器械广告批文申报、医疗器械出口销售证明办理、洁净室建设指导等提供一站式服务,技术专业,诚信服务,欢迎您咨询!
|