|
医疗器械注册广西自冶区生产企业申请二类医疗器械注册技术审评时间根据《医疗器械注册管理办法》(国家食品药品监督管理总局令第4号) 第三十三条 受理注册申请的食品药品监督管理部门应当自受理之日起3个工作日内将申报资料转交技术审评机构。技术审评机构应当在60个工作日内完成第二类医疗器械注册的技术审评工作,在90个工作日内完成第三类医疗器械注册的技术审评工作。需要外聘专家审评、药械组合产品需与药品审评机构联合审评的,所需时间不计算在内,技术审评机构应当将所需时间书面告知申请人。
广西自冶区二类医疗器械产品注册办理流程图:
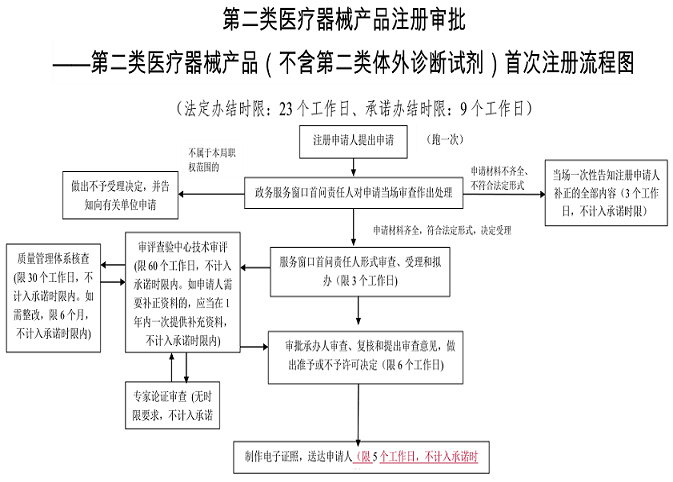
此医疗器械产品注册办理流程适合在广西辖区内申请第二类医疗器械产品(不含第二类体外诊断试剂)首次注册的企业。
进口、国内医疗器械产品注册及生产许可办理(包括:医疗器械产品注册技术文件编写、医疗器械质量管理体系建立、现场体考核查指导、设计开发文件编写指导、批记录编写指导、现场培训、生产许可申报资料编写及相关事项网上系统申报等)、一类医疗器械产品备案、生产备案、广告批文、出口销售证明办理,洁净室建设规划等事项需要协助辅导办理请您找深圳鸿远医疗器械咨询有限公司为您提供一站式专业服务!
|