|
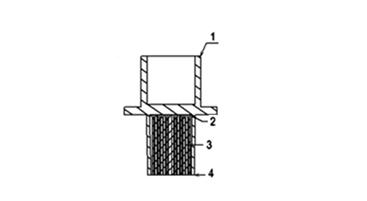
医疗器械注册证申请热湿交换器产品按照《医疗器械分类目录》(国家食品药品监督管理总局公告2017第104号)中管理类别为Ⅱ类的热湿交换器,分类编码为08-05-04(呼吸、麻醉和急救器械-呼吸、麻醉、急救设备辅助装置-热湿交换器)。通常由储水储热材料和壳体组成,包括一个进气口和一个出气口,通过保留患者呼气中部分水分和热量,并在吸气过程中将其返回到呼吸道的器械。用于提高输送给呼吸道的气体中的水分含量和温度。
医疗器械产品注册热湿交换器产品适用的相关标准,标准编号标准名称如下:
GB/T 191-2008《包装储运图示标志》
GB/T 1962.1-2015《注射器、注射针及其他医疗器械用6%(鲁尔)圆锥接头 第1部分:通用要求》
GB/T 2828.1-2012《计数抽样检验程序 第1部分:按接收质量限(AQL)检索的逐批检验抽样计划》
GB/T 14233.1-2008《医用输液、输血、注射器具检验方法 第1部分:化学分析方法》
GB/T 14233.2-2005《医用输液、输血、注射器具检验方法 第2部分:生物学试验方法》
GB/T 16886.1-2011《医疗器械生物学评价 第1部分:风险管理过程中的评价与试验》
GB/T 16886.5-2017《医疗器械生物学评价 第5部分:体外细胞毒性试验》
GB/T 16886.7-2015《医疗器械生物学评价 第7部分:环氧乙烷灭菌残留量》
GB/T 16886.10-2017《医疗器械生物学评价 第10部分:刺激与皮肤致敏试验》
YY/T 0313-2014《医用高分子产品 包装和制造商提供信息的要求》
YY/T 0466.1-2016《医疗器械 用于医疗器械标签、标记和提供信息的符号 第1部分:通用要求》
YY/T 0735.1-2009《麻醉和呼吸设备 湿化人体呼吸气体的热湿交换器(HME) 第1部分:用于最小潮气量为250mL的HME》
YY/T 0735.2-2010《麻醉和呼吸设备 用于加湿人体呼吸气体的热湿交换器(HMEs) 第2部分:用于气管切开术患者的250mL以上潮气量的HMEs》
YY/T 1040.1-2015《麻醉和呼吸设备 圆锥接头 第1部分:锥头与锥套》
YY/T 1040.2-2008《麻醉和呼吸设备 圆锥接头 第2部分:螺纹承重接头》
注:本指导原则中标准适用最新版本,下同。声称产品具有过滤功能的,应选用相应适用的标准。
上述标准包括了医疗器械注册产品技术要求中通常涉及到的标准。企业可根据产品的特点引用其他适用的国家、行业标准。
产品适用及引用标准的审查可以分两步来进行。首先对引用标准的齐全性和适宜性进行审查,也就是在编写产品技术要求时是否引用了与产品相关的国家标准、行业标准,以及引用是否准确。可以通过查阅其提交的研究资料,对是否引用了相关标准,以及所引用的标准是否适宜来进行审查。此时,应注意标准编号、标准名称是否完整规范,年代号是否有效。
其次对引用标准的采纳情况进行审查。即所引用的标准中的条款要求,是否在产品技术要求中进行了实质性的条款引用。这种引用通常采用两种方式,文字表述繁多内容复杂的可以直接引用标准及条文号,比较简单的也可以直接引述具体要求。
如有新版强制性国家标准、行业标准发布实施,产品性能指标等要求应执行最新版本的国家标准、行业标准。
医疗器械产品注册证申请产品的研究要求:
1.产品性能研究
医疗器械注册代理应详述产品技术要求中主要性能指标及检验方法的确定依据,提供采用的原因及理论基础,提供涉及的研究性资料、文献资料和标准文本。如适用的国家标准、行业标准中有不采纳的条款,应将不采纳的条款及其理由予以阐明。
应研究的产品基本性能至少包括YY/T 0735.1-2009或YY/T 0735.2-2010规定的性能。
对于声称产品具有过滤功能的,企业应提出相应安全性、有效性的要求。
潮气量小于250mL的热湿交换器,申请人应确定评价方法或者参考YY/T 0735.1-2009或YY/T 0735.2-2010,并调整试验参数。
2.生物相容性研究
医疗器械产品注册代理申请产品应描述热湿交换器与人体间接接触部件的材料,以及接触的性质和时间,参照《关于印发医疗器械生物学评价和审评指南的通知》(国食药监械〔2007〕345号)、GB/T 16886.1-2011《医疗器械生物学评价 第1部分:风险管理过程中的评价与试验》的要求对其进行生物相容性评价。
3.灭菌工艺及洁净控制工艺研究
3.1按GB 18278.1-2015《医疗保健品灭菌 湿热 第1部分:医疗器械灭菌过程的开发、确认和常规控制要求》、GB 18279.1-2015《医疗保健产品灭菌 环氧乙烷 第1部分:医疗器械灭菌过程的开发、确认和常规控制的要求》、GB/T 18279.2-2015《医疗保健产品的灭菌 环氧乙烷 第2部分:GB 18279.1应用指南》、GB 18280.1-2015《医疗器械保健产品灭菌 辐射 第1部分:医疗器械灭菌过程的开发、确认和常规控制要求》、GB 18280.2-2015《医疗保健产品灭菌 辐射 第2部分:建立灭菌剂量》、GB/T 18280.3-2015《医疗保健产品灭菌 辐射 第3部分:剂量测量指南》、GB 18281.2-2015《医疗保健产品灭菌 生物指示物 第2部分:环氧乙烷灭菌用生物指示物》、GB/T 19633.1-2015《最终灭菌医疗器械包装 第1部分:材料、无菌屏障系统和包装系统的要求》、GB/T 19633.2-2015《最终灭菌医疗器械包装 第2部分:成形、密封和装配过程确认的要求》、YY/T 1267-2015《适用于环氧乙烷灭菌的医疗器械的材料评价》或者适用其他灭菌方式材料评价的标准、YY/T 0698系列标准等要求提交灭菌研究资料。
如果灭菌方式会导致有害物质残留,应进行相关评价。如热湿交换介质等易吸附环氧乙烷,环氧乙烷残留量超标会产生相应危害。
3.2洁净供应的热湿交换器微生物限度、环境及管理要求及检查方法可结合申报产品的危险性程度和临床使用最不利情况参照GB 15982-2012《医院消毒卫生标准》及《中华人民共和国药典》提交研究资料。
4.效期和包装研究
4.1产品有效期和包装研究情况可通过实时老化或加速老化试验获得。加速老化试验可参照YY/T 0681和YY/T 0698系列标准、GB/T 19633.1-2015《最终灭菌医疗器械包装 第1部分:材料、无菌屏障系统和包装系统的要求》、GB/T 19633.2-2015《最终灭菌医疗器械包装 第2部分:成形、密封和装配过程的确认的要求》。使用的包装材料为医用级别。
4.2医疗器械注册证申请人应提交包装研究资料,依据有关国内、国际标准进行(如GB/T 19633.1、GB/T 19633.2、ISO 11607、ASTM F2475、ASTM D4169等)对包装进行分析研究和评价。直接接触产品的包装材料的选择应至少考虑以下因素:包装材料的物理化学性能;包装材料的毒理学特性;包装材料与产品的适应性;包装材料与成型和密封过程的适应性;包装材料与灭菌或洁净控制过程的适应性;包装材料所能提供的物理、化学和微生物屏障保护;包装材料与使用者使用时的要求(如无菌开启)的适应性;包装材料与标签系统的适应性;包装材料与贮存运输过程的适应性。
医疗器械注册热湿交换器产品技术要求的主要性能指标:
拟定产品技术要求应符合《医疗器械注册管理办法》和《医疗器械注册申报资料要求和批准证明文件格式》(国家食品药品监督管理总局公告2014年第43号)的相关规定,按照《医疗器械产品技术要求编写指导原则》(国家食品药品监督管理总局通告2014年第9号)要求编写。
本条款给出热湿交换器的产品基本技术性能指标,但并未给出定量要求,企业可参考相应的国家标准、行业标准,如YY/T 0735.1-2009《麻醉和呼吸设备 湿化人体呼吸气体的热湿交换器(HME) 第1部分:用于最小潮气量为250mL的HME》、YY/T 0735.2-2010《麻醉和呼吸设备 用于加湿人体呼吸气体的热湿交换器(HMEs) 第2部分:用于气管切开术患者的250mL以上潮气量的HMEs》,根据企业自身产品的技术特点制定相应的技术要求。医疗器械注册证请产品技术要求不得低于YY/T 0735.1-2009、YY/T 0735.2-2010等适用的相应国家/行业标准要求。
1.物理性能
医疗器械注册证代理申请产品一般应包括热湿交换器患者端口接头、附加端口(呼吸辅助装置的接头/呼吸附件接头、辅助端口)、水分损失(不同潮气量的水分损失应予以评价)、压降、气体泄漏、顺应性、外观等。其中气体泄漏、顺应性不适用于连接气管切开插管的热湿交换器。
2.化学性能
根据不同材料特性,由企业对化学性能提出要求。用环氧乙烷灭菌的产品应规定环氧乙烷残留量的要求。
3.微生物要求
若以无菌形式提供,应进行无菌检验。
医疗器械注册办理产品非无菌供应一次性使用的产品,若产品使用前不需要进行消毒、灭菌处理,应对其微生物限度进行评价,同时可参考《中华人民共和国药典》中微生物限度检查法进行检测。
4.若产品包含其他附加功能(如过滤性能),应结合产品功能、结构制定相关性能要求。
深圳鸿远医疗器械咨询有限公司是一家技术专业的医疗器械咨询公司,专注提供全国各地如:深圳、广州、东莞、中山、佛山、潮州、顺德、广西、上海、西安、重庆、成都等知名城市的医疗器械领域技术咨询服务。鸿远医疗器械咨询专业服务于:医疗器械产品注册证、医疗器械生产许可证、进口医疗器械注册、体外诊断试剂注册代办理咨询、一类医疗器械产品备案及生产备案代办、医疗器械经营许可证代办、二类医疗器械经营备案、医疗器械分类界定、CE认证、ISO13485认证、FDA注册、临床试验、医疗器械质量管理体系认证及体系建立与过程确认文件建立(ISO9001, ISO13485, GMP, CE,QSR820,CMDCAS);产品技术要求制订、技术文件、临床试验及免临床同类产品比对比资料编写、注册资料编写辅导、电磁兼容预测整改、医疗器械广告批文申报、医疗器械出口销售证明办理、洁净室建设指导等提供一站式服务,技术专业,诚信服务,欢迎您咨询!
|