医疗器械注册受理条件及标准:
1、申报注册的产品已经列入《总局关于发布医疗器械分类目录的公告》(2017年第104号)的附件《医疗器械分类目录》,且管理类别为第二类。(注:对新研制的尚未列入分类目录的医疗器械,申请人可以直接向国家食品药品监督管理总局申请第三类医疗器械产品注册,也可以依据分类规则判断产品类别并向国家食品药品监督管理总局申请类别确认后,申请产品注册或者办理产品备案。)
2、申请人应当是在广东省辖区范围依法进行登记的企业(医疗器械注册人制度试点申请人要求另行规定)。
3、申请人建立与产品研制、生产有关的质量管理体系,并保持有效运行。申请注册时样品不得委托其他企业生产,按照创新医疗器械特别审批程序审批的或符合医疗器械注册人制度试点要求的产品除外。
4、办理医疗器械注册事务的人员应当具有相应的专业知识,熟悉医疗器械注册或者备案管理的法律、法规、规章和技术要求,如:《医疗器械监督管理条例》、《医疗器械注册与备案管理办法》、《医疗器械分类规则》、《关于进一步做好医疗器械产品分类界定工作的通知》、《关于发布医疗器械产品技术要求编写指导原则的通告》、《医疗器械临床试验规定》、《医疗器械临床评价技术指导原则》、《医疗器械说明书和标签管理规定》、食品药品监管总局关于实施《医疗器械注册与备案管理办法》有关事项的通知、《关于公布医疗器械注册申报资料要求和批准证明文件格式的公告》等。
5、申请人申请注册,应当遵循医疗器械安全有效基本要求,保证研制过程规范,所有数据真实、完整和可溯源。
6、申请注册的资料应当使用中文。根据外文资料翻译的,应当同时提供原文。引用未公开发表的文献资料时,应当提供资料所有者许可使用的证明文件。申请人对资料的真实性负责。
7、广东省医疗器械注册人制度的注册申请人还应同时符合以下条件:
(1)住所位于广东省行政区域内,可以是企业、研发机构和科研人员;
(2)委托在广东省行政区域内依法设立的企业生产本产品;
(3)应当配备专职的法规事务、质量管理、上市后事务等相关人员,以上人员应具有相应的专业背景和工作经验,并不得相互兼职;
(4)具备医疗器械全生命周期管理能力,有对质量管理体系进行评估、审核和监督的人员和条件;
(5)具备承担医疗器械质量安全责任的能力,确保研制过程规范,所有数据真实、完整、可追溯。 注:纳税信用A级纳税人、安全生产领域守信生产经营单位及其有关人员、海关高级认证企业,在办理第二类医疗器械产品注册时,可参照《广东省药品监督管理局第二类医疗器械优先审批程序》办理。
医疗器械注册办理流程图:
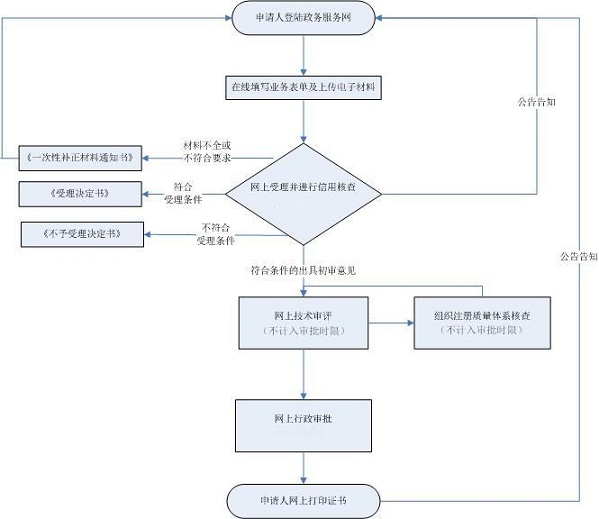
医疗器械注册证办理步骤:
一、收件
1.申请事项依法不需要取得行政许可的,应当场告知申请人不予受理并出具不予受理通知书;
2.申请事项依法不属于本行政机关职权范围的应当场出具不予受理通知书,并在受理通知书上告知申请人向相关行政机关提出申请;
3.申请人隐瞒有关情况或者提供虚假材料申请的,出具不予受理通知书。
4.不能当场审查不齐全或不符合法定形式的,当场出具收件通知书,五日内审查材料不齐全或不符合法定形式的,出具包含具体补正要求的一次性告知通知书;
5.能当场判断申请材料需要补正的,应当场出具一次性告知通知书。
审批标准:
1.核对申请人是否符合申请条件;
2.依据办事指南中材料清单逐一核对是否齐全;
3.核对每个材料是否涵盖材料要求中涉及的内容和要素。
二、受理
办理结果:
1.能当场受理或通过当场补正达到受理条件的,直接进入受理步骤,当场出具受理通知书;
2.根据一次性告知通知书内容进行补正后达到受理条件的,出具决定受理通知书;
3.收件之日起5个工作日内未收到一次性告知通知书的,从收件之日起即为受理。
审批标准:
1.核对申请人是否符合申请条件;
2.依据办事指南中材料清单逐一核对是否齐全;
3.核对每个材料是否涵盖材料要求中涉及的内容和要素。
三、审查
办理结果:提出初步意见,转入决定步骤。
审批标准:技术审评意见是否清晰,结论是否明确。
四、决定
办理结果:
1.符合规定的,准予行政许可。
2.不符合规定的,不准予行政许可。
审批标准:复核审查步骤阶段提出的初步意见。
五、制证
办理结果:准予行政许可决定书 不准予行政许可决定书
六、送达
办理结果:1.准予行政许可的颁发《准予行政许可决定书》 2.不予行政许可的颁发《不予行政许可决定书》
送达方式:窗口领取、代理人送达、委托送达、公告送达、邮寄送达
医疗器械产品注册 申请材料依据《医疗器械注册与备案管理办法》国家市场监督管理总局令第47号第五十二条第一款第(一)项、第(二)项、第(三)项、第(四)项、第(五)项、第(六)项、第(七)项申请人应当在完成支持医疗器械注册的安全性、有效性研究,做好接受质量管理体系核查的准备后,提出医疗器械注册申请,并按照相关要求,通过在线注册申请等途径向药品监督管理部门提交下列注册申请资料: 产品风险分析资料; 产品技术要求; 产品检验报告; 临床评价资料; 产品说明书以及标签样稿; 与产品研制、生产有关的质量管理体系文件; 证明产品安全、有效所需的其他资料。
申请材料目录:
1、医疗器械注册申请表
2、监管信息
3、综述资料
4、非临床资料
5、临床评价资料
6、产品说明书和标签样稿
7、质量管理体系文件
8、营业执照
广东省二类医疗器械注册收费标准:广东省第二类医疗器械产品首次注册费57260元。
二类医疗器械注册证办理依据法律法规《医疗器械监督管理条例》中华人民共和国国务院令第739号:
第十六条第一款、第二款、第三款,申请第二类医疗器械产品注册,注册申请人应当向所在地省、自治区、直辖市人民政府药品监督管理部门提交注册申请资料。申请第三类医疗器械产品注册,注册申请人应当向国务院药品监督管理部门提交注册医疗器械申请资料。 向我国境内出口第二类、第三类医疗器械的境外注册申请人,由其指定的我国境内企业法人向国务院药品监督管理部门提交注册申请资料和注册申请人所在国(地区)主管部门准许该医疗器械上市销售的证明文件。未在境外上市的创新医疗器械,可以不提交注册申请人所在国(地区)主管部门准许该医疗器械上市销售的证明文件。 国务院药品监督管理部门应当对医疗器械注册审查程序和要求作出规定,并加强对省、自治区、直辖市人民政府药品监督管理部门注册审查工作的监督指导。
第十七条第一款、第二款、第三款
受理注册申请的药品监督管理部门应当对医疗器械的安全性、有效性以及注册申请人保证医疗器械安全、有效的质量管理能力等进行审查。 受理注册申请的药品监督管理部门应当自受理注册申请之日起3个工作日内将注册申请资料转交技术审评机构。技术审评机构应当在完成技术审评后,将审评意见提交受理注册申请的药品监督管理部门作为审批的依据。 受理注册申请的药品监督管理部门在组织对医疗器械的技术审评时认为有必要对质量管理体系进行核查的,应当组织开展质量管理体系核查。
第十八条第一款、第二款
受理注册申请的药品监督管理部门应当自收到审评意见之日起20个工作日内作出决定。对符合条件的,准予注册并发给医疗器械注册证;对不符合条件的,不予注册并书面说明理由。 受理注册申请的药品监督管理部门应当自医疗器械准予注册之日起5个工作日内,通过国务院药品监督管理部门在线政务服务平台向社会公布注册有关信息。
第十九条第一款、第二款
对用于治疗罕见疾病、严重危及生命且尚无有效治疗手段的疾病和应对公共卫生事件等急需的医疗器械,受理注册申请的药品监督管理部门可以作出附条件批准决定,并在医疗器械注册证中载明相关事项。 出现特别重大突发公共卫生事件或者其他严重威胁公众健康的紧急事件,国务院卫生主管部门根据预防、控制事件的需要提出紧急使用医疗器械的建议,经国务院药品监督管理部门组织论证同意后可以在一定范围和期限内紧急使用。
第二十一条第一款
已注册的第二类、第三类医疗器械产品,其设计、原材料、生产工艺、适用范围、使用方法等发生实质性变化,有可能影响该医疗器械安全、有效的,注册人应当向原注册部门申请办理变更注册手续;发生其他变化的,应当按照国务院药品监督管理部门的规定备案或者报告。
第二十二条第一款、第二款、第三款第(一)项、第(二)项、第(三)项
医疗器械产品注册证有效期为5年。有效期届满需要延续注册的,应当在有效期届满6个月前向原注册部门提出延续注册的申请。 除有本条第三款规定情形外,接到延续注册申请的药品监督管理部门应当在医疗器械注册证有效期届满前作出准予延续的决定。逾期未作决定的,视为准予延续。 有下列情形之一的,不予延续注册: 未在规定期限内提出延续注册申请; 医疗器械强制性标准已经修订,申请延续注册的医疗器械不能达到新要求; 附条件批准的医疗器械,未在规定期限内完成医疗器械注册证载明事项。
办理医疗器械注册依据《医疗器械注册与备案管理办法》国家市场监督管理总局令第47号:
第八条第一款、第二款、第三款、第四款、第五款、第六款
一类医疗器械实行产品备案管理。第二类、第三类医疗器械实行产品注册管理。 境内第一类医疗器械备案,备案人向设区的市级负责药品监督管理的部门提交备案资料。 境内第二类医疗器械由省、自治区、直辖市药品监督管理部门审查,批准后发给医疗器械注册证。 境内第三类医疗器械由国家药品监督管理局审查,批准后发给医疗器械注册证。 进口第一类医疗器械备案,备案人向国家药品监督管理局提交备案资料。 进口第二类、第三类医疗器械由国家药品监督管理局审查,批准后发给医疗器械注册证。
第四十八条第一款、第二款
境内第三类医疗器械质量管理体系核查,由国家局器械审评中心通知申请人所在地的省、自治区、直辖市药品监督管理部门开展。 境内第二类医疗器械质量管理体系核查,由申请人所在地的省、自治区、直辖市药品监督管理部门组织开展。
第五十八条第一款、第二款
受理注册申请的药品监督管理部门应当在技术审评结束后,作出是否批准的决定。对符合安全、有效、质量可控要求的,准予注册,发给医疗器械注册证,经过核准的产品技术要求以附件形式发给申请人。对不予注册的,应当书面说明理由,并同时告知申请人享有依法申请行政复议或者提起行政诉讼的权利。 医疗器械注册证有效期为5年。
第七十九条第一款、第二款、第三款、第四款
注册人应当主动开展医疗器械上市后研究,对医疗器械的安全性、有效性和质量可控性进行进一步确认,加强对已上市医疗器械的持续管理。 已注册的第二类、第三类医疗器械产品,其设计、原材料、生产工艺、适用范围、使用方法等发生实质性变化,有可能影响该医疗器械安全、有效的,注册人应当向原注册部门申请办理变更注册手续;发生其他变化的,应当在变化之日起30日内向原注册部门备案。 注册证载明的产品名称、型号、规格、结构及组成、适用范围、产品技术要求、进口医疗器械的生产地址等,属于前款规定的需要办理医疗器械变更注册的事项。注册人名称和住所、代理人名称和住所等,属于前款规定的需要备案的事项。境内医疗器械生产地址变更的,注册人应当在办理相应的生产许可变更后办理备案。 发生其他变化的,注册人应当按照质量管理体系要求做好相关工作,并按照规定向药品监督管理部门报告。
第八十二条第一款、第二款
医疗器械注册证有效期届满需要延续注册的,注册人应当在医疗器械注册证有效期届满6个月前,向原注册部门申请延续注册,并按照相关要求提交申请资料。 除有本办法第八十三条规定情形外,接到延续注册申请的药品监督管理部门应当在医疗器械注册证有效期届满前作出准予延续的决定。逾期未作决定的,视为准予延续。
第九十二条第一款第(一)项、第(二)项、第(三)项
医疗器械注册技术审评时限,按照以下规定执行: 医疗器械临床试验申请的技术审评时限为60日,申请资料补正后的技术审评时限为40日; 第二类医疗器械注册申请、变更注册申请、延续注册申请的技术审评时限为60日,申请资料补正后的技术审评时限为60日; 第三类医疗器械注册申请、变更注册申请、延续注册申请的技术审评时限为90日,申请资料补正后的技术审评时限为60日。
第九十四条第一款
受理注册申请的药品监督管理部门应当自收到审评意见之日起20日内作出决定。
第九十五条第一款
药品监督管理部门应当自作出医疗器械注册审批决定之日起10日内颁发、送达有关行政许可证件。
深圳鸿远医疗器械咨询有限公司是一家技术专业的
医疗器械咨询公司,专注提供全国各地如:深圳、广州、东莞、中山、佛山、潮州、顺德、上海、广西、福建、西安、重庆、成都等知名城市的医疗器械领域技术咨询服务。鸿远医疗器械咨询专业服务于:
国内医疗器械产品注册证、医疗器械生产许可证、进口医疗器械注册、一类医疗器械产品备案及生产备案、医疗器械经营许可证、二类医疗器械经营备案凭证等代办理咨询、CE认证、ISO13485认证、FDA注册、临床试验、医疗器械质量管理体系建立与过程确认文件建立(ISO9001, ISO13485, GMP, CE,QSR820,CMDCAS);产品技术要求制订、技术文件、临床试验及免临床同类产品比对比资料编写、注册申报资料编写、电磁兼容预测整改、医疗器械广告批文申报、医疗器械出口销售证明办理等服务,欢迎您咨询!